Uma nova formulação sólida, oral, em estágio de desenvolvimento e candidata a ser um medicamento genérico (teste), contém insumo farmacêutico ativo de baixa solubilidade em água e se mostrou, na curva de biodisponibilidade (tempo versus concentração plasmática, Figura 1) fora da faixa de aceitação (intervalo entre a concentração mínima efetiva e máxima de segurança), em comparação ao medicamento referência.
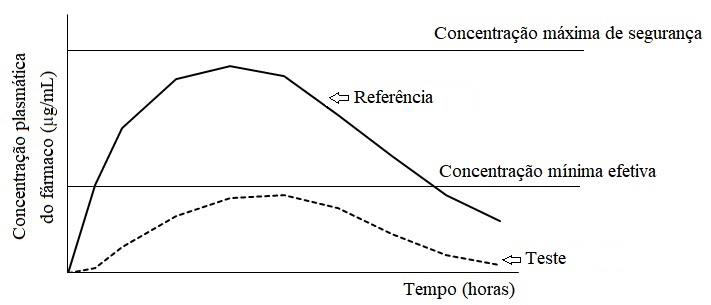
Figura 1 – Curva de biodisponibilidade do medicamento em Teste (linha pontilhada) em compração ao medicamento referência (linha contínua).
Uma possibilidade de reformulação farmacotécnica para solucionar o problema de biodisponibilidade do medicamento em teste e evitar a recusa do registro sanitário desse novo produto pode ser:
O aumento da concentração do lubrificante na formulação.
A micronização do insumo farmacêutico ativo que o compõe.
A administração do dobro da dose nos pacientes.
O desenvolvimento de uma formulação líquida oral.
A diminuição do peso médio da formulação sólida oral.