A frase “semelhante dissolve semelhante” é muito utilizada na química para justificar a solubilidade dos compostos. A solubilidade também pode ser quimicamente justificada através das interações intermoleculares (forças de atração) semelhantes, existentes entre soluto e solvente. Considere as vitaminas K3 e B7 , cujas estruturas estão representadas a seguir.
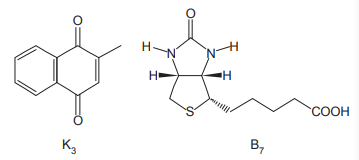
No que concerne à solubilidade em água, verifica-se que a vitamina
K3 é mais solúvel, devido às interações dipolo-dipolo que ocorrem com moléculas de água.
K3 é mais solúvel, devido às interações de ligação de hidrogênio que ocorrem com moléculas de água.
K3 é mais solúvel, devido às interações de Van der Waals que ocorrem com moléculas de água.
B7 é mais solúvel, devido às interações de ligação de hidrogênio que ocorrem com moléculas de água.
B7 é mais solúvel, devido às interações de Van der Waals que ocorrem com moléculas de água.