38
Q3510249
Teclas de Atalhos
Compartilhar
O diborano (B2H6) é um hidreto de boro altamente reativo, sendo considerado um possível combustível e propelente de foguetes em programas espaciais. O cálculo da energia envolvida na síntese de um mol de diborano pode ser feito utilizando-se a lei de Hess. Considere as equações das seguintes reações:
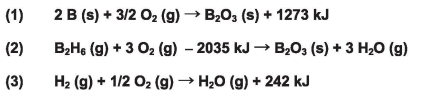
Com base nessas reações e nos calores envolvidos nos processos, são feitas as seguintes afirmações:
|- A reação número dois é exotérmica e o ΔH =- 2035 kJ.
Il — As três reações são exotérmicas.
Ill - A entalpia de formação do diborano é +36 kJ mol-1.
Das afirmativas feitas, está(ão) correta(s) apenas
A
I.
B
II.
C
III.
D
I e II.
E
I, II e III.