A molécula de oxigênio O2 é paramagnética, ou seja, possui tendência de se alinhar paralelamente a um campo magnético externo. Apesar de muito úteis, as estruturas de Lewis nem sempre descrevem adequadamente todas as características de uma substância. Um modelo muito mais refinado é o estudo dos diagramas de orbitais moleculares (DOM). São apresentados, a seguir, a estrutura de Lewis e o DOM para a molécula de oxigênio.
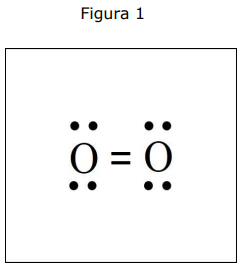
(Fonte: BEAVER, Scott. O2 Lewis
Structure. 2024. Disponível em:
https://learnwithdrscott.com/o2-lewisstructure/. Acesso em 30 out. 2024.)
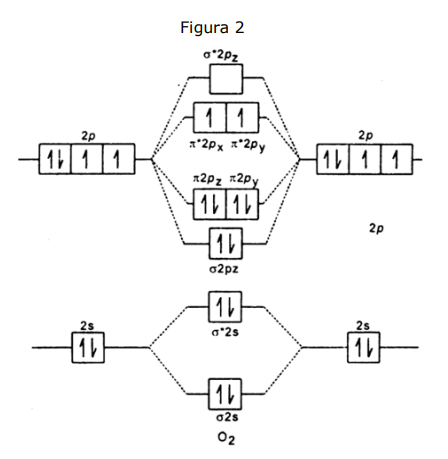
(Fonte: COSTA, João. Soluções Química - Semana 140.
Disponível em:https://noic.com.br/solucoes-quimica-
semana-140/. Acesso em 30 out. 2024.)
A partir de ambos os modelos, são feitas as seguintes afirmações:
I. A estrutura de Lewis apresentada não consegue prever comportamento paramagnético para a molécula de oxigênio, uma vez que não apresenta elétrons desemparelhados em sua estrutura.
II. A ordem de ligação pelo modelo dos orbitais moleculares para a molécula de oxigênio é 2, a mesma da estrutura de Lewis.
III. A adição de um elétron na molécula de O2, formando o íon superóxido O2 - , acarretaria um aumento da ordem de ligação da estrutura.
Com base nas afirmações sobre os modelos apresentados, está(ão) correta(s) apenas a(s) afirmativa(s)
I.
III.
I e II.
II e III.